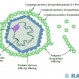
La diagnosi di infezione da Virus dell’Epatite C (HCV) può essere effettuata al giorno d’oggi con differenti e specifiche tecniche, ciascuna caratterizzata da pregi e difetti che le rendono più o meno adatte a seconda della situazione. In passato i Centers for Disease Control (CDC) avevano proposto un algoritmo al fine di promuovere un uso corretto e sistematico delle risorse a disposizione nei laboratori durante l’analisi di potenziali casi di infezione da HCV. Ad oggi queste linee guida rimangono ancora un saldo punto di riferimento durante la fase decisionale per le analisi a cui sottoporre i pazienti potenzialmente affetti da HCV. Al loro interno sono riportati alcuni dei saggi maggiormente diffusi e conosciuti per la diagnosi dell’HCV: il saggio immuno-assorbente legato ad un enzima (ELISA) è sicuramente quello maggiormente utilizzato; caratterizzato da un’elevata sensibilità e specificità grazie alla capacità d’interagire con multipli antigeni virali, è tuttavia caratterizzato da un basso valore predittivo positivo. Un’altra ben nota famiglia di test è quella dei point-of-care (POCT); sviluppati per fornire delle rapide diagnosi senza l’uso di laboratori clinici, basano il loro funzionamento sull’identificazione degli stessi antigeni virali dell’ELISA ed hanno già dimostrato performance simili agli ELISA durante alcune valutazioni cliniche dei CDC. D’altro canto la Food and Drug Administration (FDA), responsabile negli Stati Uniti della supervisione e controllo dei differenti beni per la salute della comunità, ne ha approvato uno soltanto fra quelli proposti. Poi ci sono i saggi d’immunofissazione ricombinante (RIBA), altamente specifici ma anche costosi ed inefficienti; i test degli acidi nucleici (NAT), altamente specifici e selettivi, utilizzati come saggi di conferma per le infezioni da HCV benché nessuno di questi abbia ancora ricevuto un’approvazione da parte delle agenzie regolatrici per la diagnosi delle infezioni da HCV; ed infine i saggi dell’antigene del core dell’HCV, con un principio di funzionamento simile al NAT richiede una elaborazione minore dei saggi molecolari.
6 marzo 2017
Aggiornamento sulle linee guida per la diagnosi di infezione da parte del virus dell’Epatite C
Testing for HCV Infection: An Update of Guidance for Clinicians and Laboratorians
Centers for Disease Control and Prevention, May 2013
https://www.cdc.gov/mmwr/pdf/wk/mm62e0507a2.pdf